2022年全國進入優(yōu)先審批通道醫(yī)械產品數量達117件
一、總體概況
根據眾成數科統(tǒng)計,截至2022年12月31日進入國家優(yōu)先醫(yī)療器械特別審查程序的Ⅱ、Ⅲ類產品數量累計達1144件。其中,2022年進入國家優(yōu)先審批通道醫(yī)械產品數量為117件,同比下降43.75%。2022年獲批數量為76件,10件為Ⅲ類產品,66件為Ⅱ類產品。
圖1 2017-2022年進入和獲批我國優(yōu)先醫(yī)療器械特別審查Ⅱ、Ⅲ類產品數量
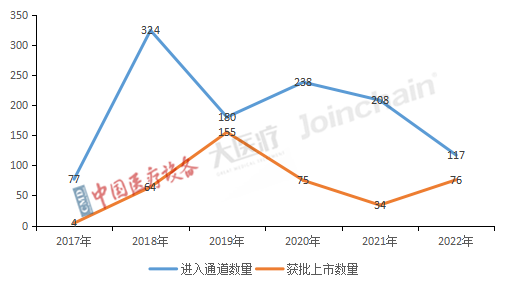
數據來源:中國醫(yī)療設備、大醫(yī)療、眾成數科
二、地域分布
從產品屬地省市分布來看,進入II類優(yōu)先審批通道產品數量最多為天津市,以50件高居第一位,廣東省以19件居第二位,重慶市以13件居第三位。III類產品則分布在廣東省、江蘇省和上海市,均為2件。
圖2 2022年全國進入Ⅱ類、Ⅲ類醫(yī)療器械優(yōu)先審批產品省份分布
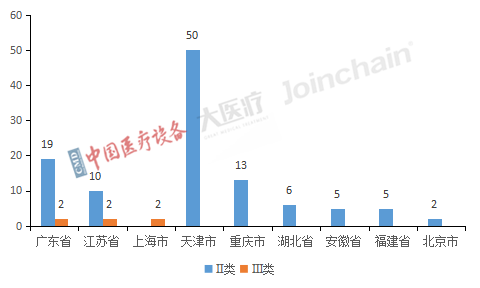
數據來源:中國醫(yī)療設備、大醫(yī)療、眾成數科
2022年獲得優(yōu)先審批的醫(yī)械產品共76件,分布在12個省份,獲批最多的是安徽省和天津市,均有17個II類產品獲得優(yōu)先審批,重慶市共有12個II類產品獲得優(yōu)先審批。此外,上海市有3個III類產品獲得優(yōu)先審批,江蘇省、福建省、山東省和浙江省均有1個III類產品獲得優(yōu)先審批。
圖3 2022年全國獲優(yōu)先審批Ⅱ、Ⅲ類醫(yī)療器械產品省份分布
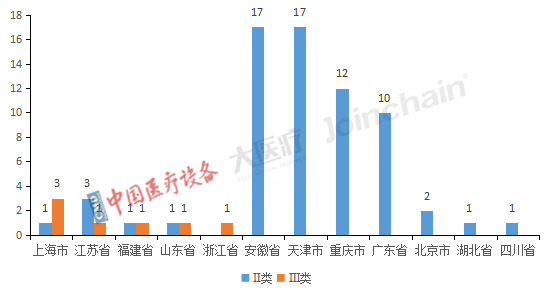
數據來源:中國醫(yī)療設備、大醫(yī)療、眾成數科
三、細分領域
從細分領域來看,2022年獲批數量最多的是體外診斷試劑,共有15件II類產品和2件III類產品獲批。獲批的III類產品還有醫(yī)用成像器械(4件)、有源手術器械(1件)、物理治療器械(2件)、無源植入器械(1件)。臨床檢驗器械和醫(yī)用成像器械獲批的II類產品數量分別為12件、8件。
圖4 2022年全國獲優(yōu)先審批Ⅱ類、Ⅲ類醫(yī)療器械產品類別分布
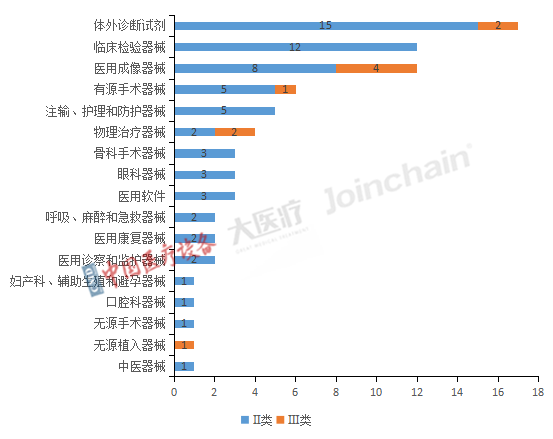
數據來源:中國醫(yī)療設備、大醫(yī)療、眾成數科
四、典型企業(yè)
2022年獲批的76件優(yōu)先產品中,分別來自53家企業(yè)。上海聯(lián)影醫(yī)療科技股份有限公司有3項Ⅲ類優(yōu)先醫(yī)療器械產品獲得審批,Uptake Medical B.V.有2項Ⅲ類優(yōu)先醫(yī)療器械產品獲得審批。雅博捷銳(重慶)醫(yī)療科技有限公司有5項Ⅱ類優(yōu)先醫(yī)療器械產品獲得審批,安徽佳創(chuàng)生物科技有限公司有4項Ⅱ類優(yōu)先醫(yī)療器械產品獲得審批。
表1 2022年獲批Ⅲ類優(yōu)先醫(yī)療器械注冊證的典型企業(yè)及其主要產品名稱
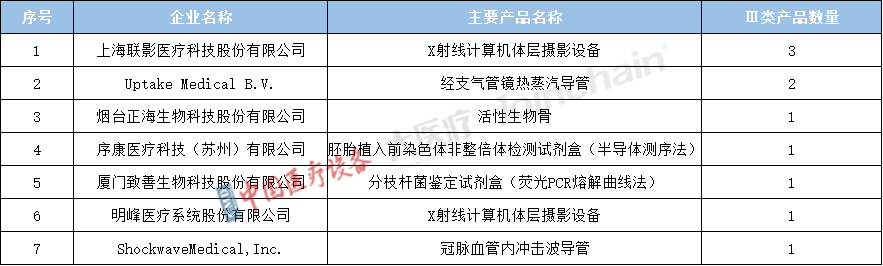
數據來源:中國醫(yī)療設備、大醫(yī)療、眾成數科
表2 2022年獲批Ⅱ類優(yōu)先醫(yī)療器械注冊證的典型企業(yè)及其主要產品名稱
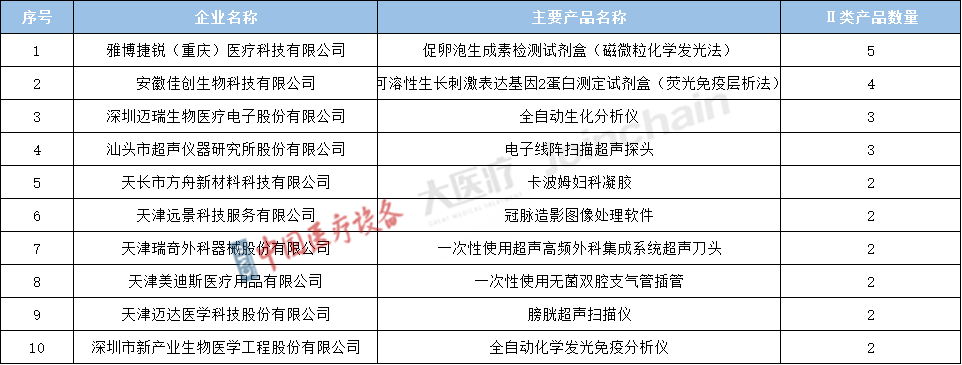
數據來源:中國醫(yī)療設備、大醫(yī)療、眾成數科



 互聯(lián)網備案號 12019202000405
互聯(lián)網備案號 12019202000405